Santé : la nouvelle réglementation européenne fait grincer les dents du secteur du dispositif médical Leave a comment

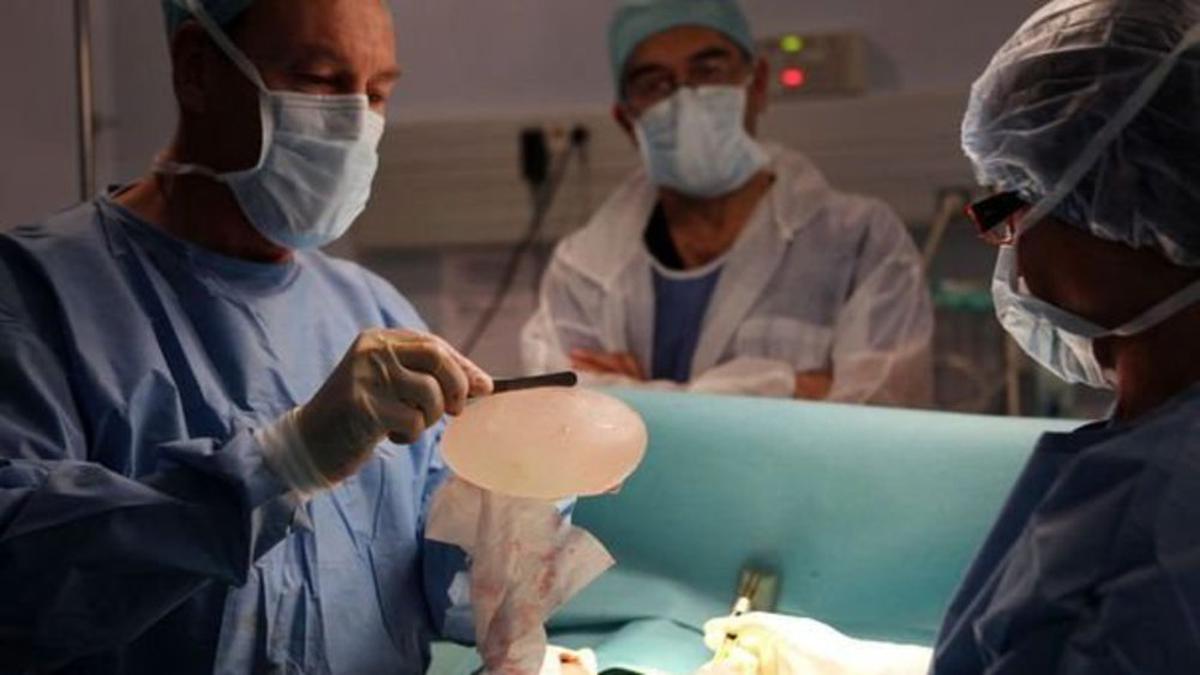
Un secteur qui n’est pas à l’abri des polémiques : on se souvient au début des années 2010 du scandale des prothèses mammaires défectueuses PIP, commercialisées par l’entrepreneur Jean-Claude Mas. Dans la foulée, l’organisme certificateur allemand de ces prothèses, TÜV, avait été condamné en France à indemniser des milliers de plaignantes.
« L’affaire des implants PIP a mis au jour une difficulté d’application de certaines règles par les organismes notifiés » chargés de certifier les produits, reconnaît Cécile Vaugelade, directrice des affaires technico-réglementaires du Snitem, le syndicat professionnel du secteur.
25 000 certificats à délivrer
Pour mettre de l’ordre, la Commission européenne a adopté en 2017 un règlement visant à « établir un cadre réglementaire rigoureux » pour les dispositifs médicaux, « qui garantisse un niveau élevé de sécurité et de protection de la santé tout en favorisant l’innovation ». Ce règlement est applicable depuis le 26 mai 2021, avec toutefois une période de grâce jusqu’à mai 2024. Mais pour les producteurs de dispositifs, même ainsi prolongé, le délai est trop court.
En effet, tous les dispositifs médicaux déjà commercialisés doivent de nouveau être certifiés. Or il existe quelque 500 000 dispositifs sur le marché, couverts par 25 000 certificats, explique le Snitem, qui demande un report de la période de grâce de deux ans pour les dispositifs de plus haute classe de risque, et de quatre ans pour les autres. « Sur les 25 000 certificats, seul un millier ont été recertifiés jusqu’à présent », insiste Mme Vaugelade.
Pour compliquer les choses, les organismes chargés d’examiner les dispositifs doivent se faire de nouveau habiliter au titre de cette nouvelle réglementation. Un processus long et complexe, qui fait qu’actuellement, 27 organismes ont été habilités dans l’Union européenne, contre le double auparavant. En France, seul un organisme, GMED, a reçu le précieux sésame.
Possibles retraits du marché
Avec le risque que des produits soient retirés du marché, alerte le secteur. Des inquiétudes entendues par les autorités sanitaires françaises.
« Au niveau national, la France a accompagné, en même temps que la désignation de l’organisme notifié GMED, une augmentation de ses effectifs pour accroître sa capacité de traitement pour les TPE et PME françaises », indique la Direction générale de la santé dans un courriel à l’AFP. L’autorité précise aussi que le gouvernement a « mobilisé des crédits publics » pour mettre en place un guichet d’accompagnement des TPE et PME dans leurs démarches.